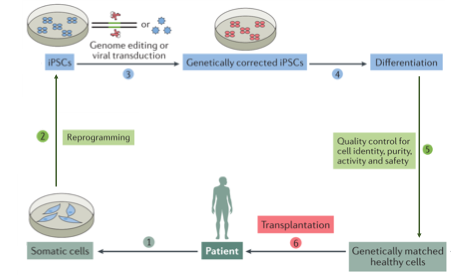
基于iPSC的自體細胞治療
(Shi, Y., et al. Nat Rev Drug Discov, 2017)
基于iPSC的自體細胞治療
iPSC具有無限擴增的能力,并且可以分化為成體所有細胞類型,可為再生醫學提供無限細胞來源。結合基因修飾技術,我們可以在獲得病人自身的iPSC后,修復病人iPSC基因組中的突變,分化為疾病相關細胞類型,然后移植給病人(如上圖)。
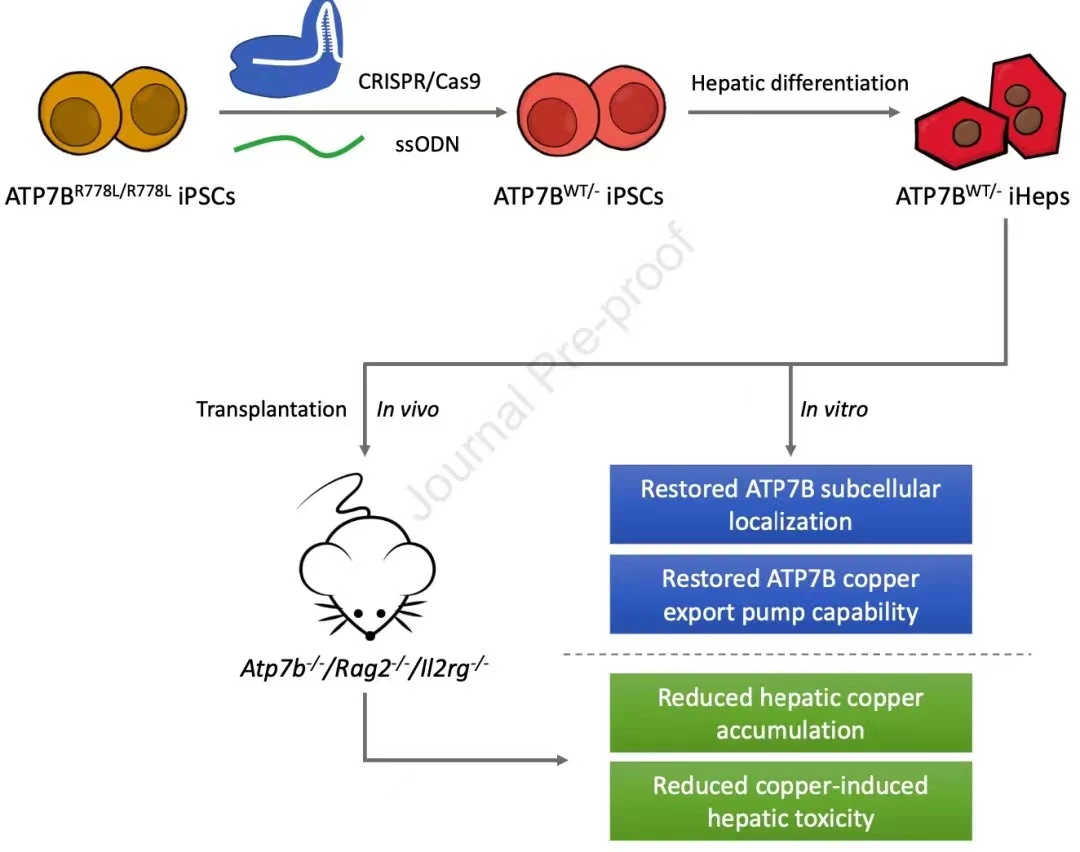
? 項目概覽
(Rui Wei et al., JHEP Reports, 2021 )
概念驗證:基因修復后的iPSC來源肝細胞治療肝豆狀核變性
病因
Disease mechanism
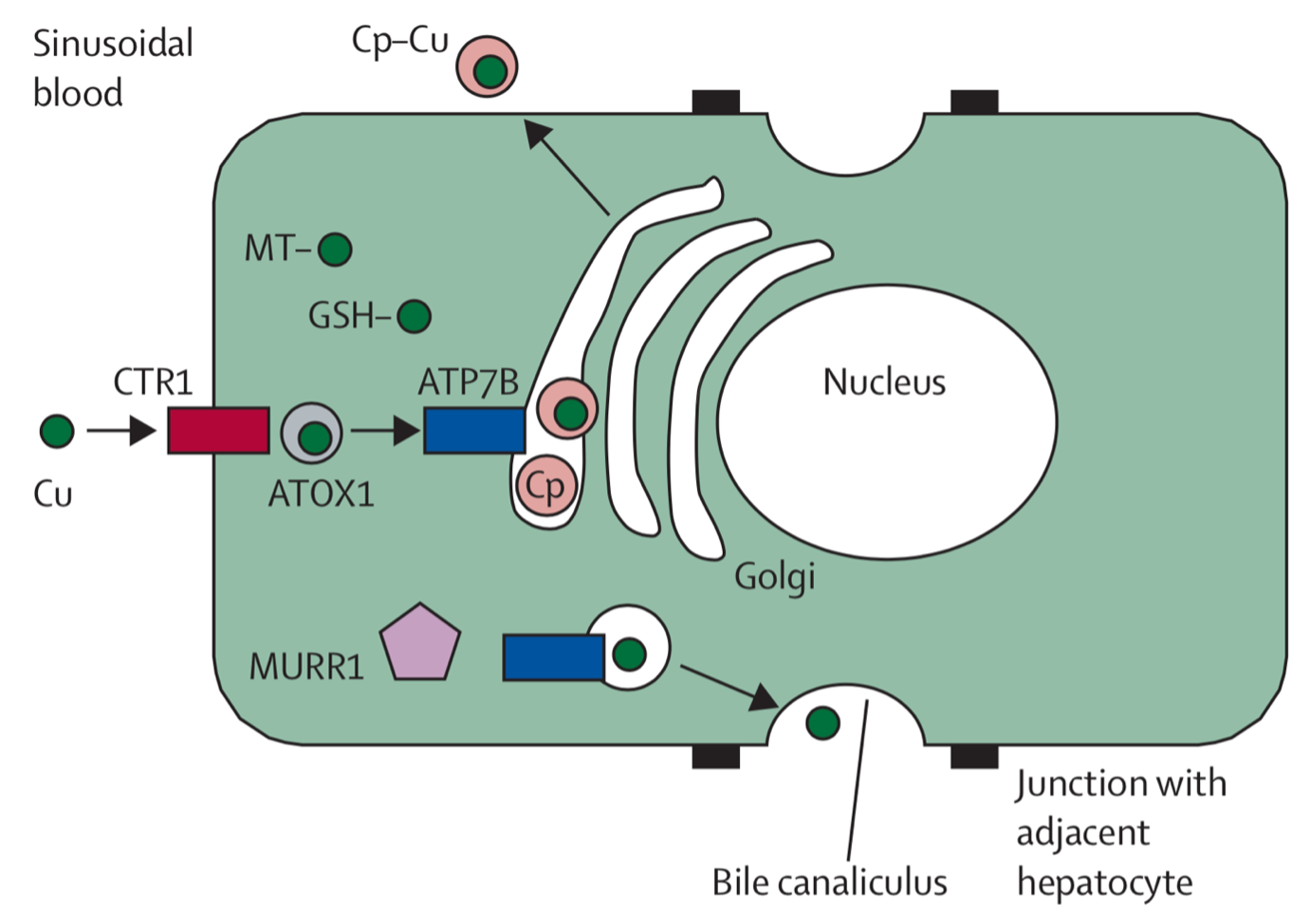
圖1 Copper Metabolism and ATP7B
(Aftab Ala et al., The lancet, 2007)
診斷和治療
Diagnosis and Treatment

? 表1 現有治療WD的藥物5
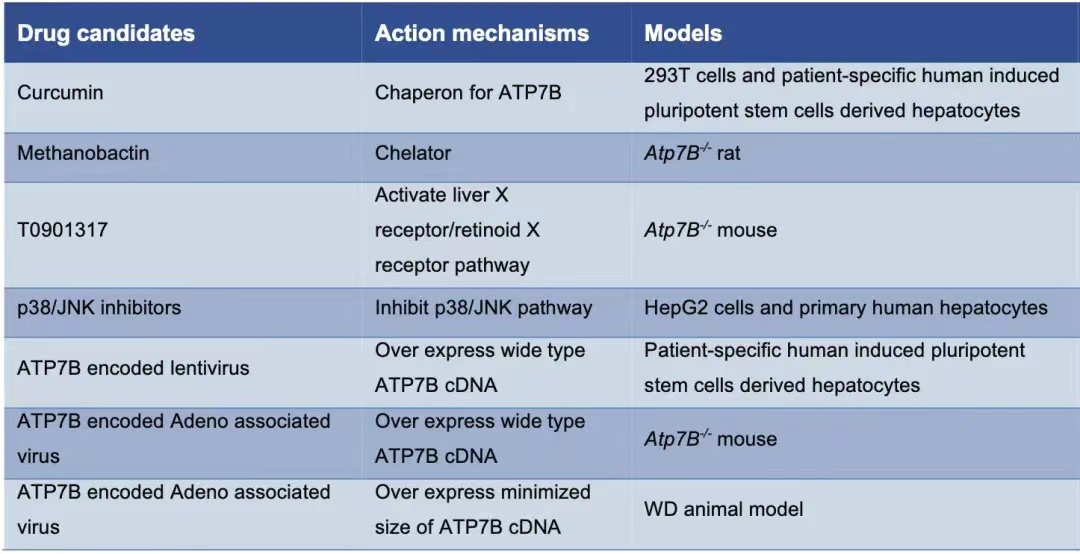
? 表2 治療WD的潛在療法5
基于iPSC的創新療法
Cell Therapy

圖3. 利用CRISPR/Cas9和ssODN修復R778L突變
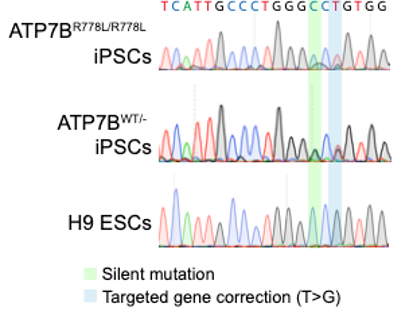
圖4. Sanger測序確認R778L被修復(雜合)
全文鏈接6:
// 參考文獻 //
1. 中華醫學會神經病學分會帕金森病及運動障礙學組. 肝豆狀核變性的診斷與治療指南. 中華神經外科雜志. 2008;41:566-569.
2. Fernandes J, Saudubray J-M, Van den Berghe G and Walter JH. Inborn metabolic diseases: diagnosis and treatment: Springer Science & Business Media; 2006.
3. 張舒揚,趙玉沛, 罕見病診療指南. 2019版, 北京: 人民衛生出版社.2019.
4. orio R, D'Ambrosi M, Marcellini M, Barbera C, Maggiore G, Zancan L, Giacchino R, Vajro P, Marazzi MG, Francavilla R, Michielutti F, Resti M, Frediani T, Pastore M, Mazzarella G, Fusco G, Cirillo F, Vegnente A, Hepatology Committee of Italian Society of Paediatric Gastroenterology H and Nutrition. Serum transaminases in children with Wilson's disease. J Pediatr Gastroenterol
Nutr. 2004;39:331-6.
5. Jiayin Yang, PhD thesis. HKU
6. Wei R, Yang J, Cheng CW, Ho WI, Li N, Hu Y, Hong X, Fu J, Yang B, Liu Y, Jiang L, Lai WH, Au KW, Tsang WL, Tse YL, Ng KM, Esteban MA, Tse HF, CRISPR-targeted genome editing of human induced pluripotent stem cell-derived hepatocytes for the treatment of Wilson’s disease, JHEP Reports (2021), doi: https://doi.org/10.1016/j.jhepr.2021.100389.
編輯:Jianquan Zhang